Pieni pikatutkimus _laillisten_ hampputuotteiden vaikutuksista ja vaikutusmekanismeista 2024-12
Pieni tutkimusrääpäisy Hampputuoteiden
terveysvaikutusmekanismeista
Elimistön homeostaasissa, yksilössä tuntuu olevan valmiudet palautumiseen ja monin tavoin eheytymiseen. Se on toiveikas hyvinvoinnin tila, jossa henkilö voi olla sisäisen syvän rauhallisuuden tilassa. Tämä edellyttää myös olemisen mielentilassa saavutettavaa mielen tasapainotilaa ja keinoja on sen tasapainottamiseen, kuten tiedostava hengitys ja siihen kyllä löytyy ohjelmansa, kunhan etsitään.
Homeostaasiin päästään käyttämällä ruokia ja tuotteita, jossa on yleisesti puuttuvia vitaaliaineita sisältävä mineraali-, vitamiini- , probiootti- öljykoostumus- jne, spektri. Tämä on optimaalista mahdollisimman monenlaisten tapausten puutosoireille, mutta pysyväislääkkeeksi lisäravinteista ei ole niiden annostelun vaikeuden vuoksi. Jossain vaiheessa tämä tuotteen potilaan tilaa korjaava spektri menee ylikorjatuksi ja siitä en nyt tiedä tutkimuksia ainakaan kannaway tuotteiden suhteen.
Ainut tuote, jota suosittelen pysyväislisäravinteena huoletta ihmisille on hyvänlaatuisten saven-suolan ja veden ja vetyveden kohtuullinen käyttö, koska "Maasta olet sinä tullut" ja varemmin merestä. Elimistön tehokkaan tasapainotilaan pääsyn vuoksi suosittelen vaihtelua vastaavien koivuntuhkan, petun ( Männyn kuori tms.), pakurin, sialiitin tai humushapon mineraalikantaa sisältävillä tuotteilla Mineralisaation parantamiseksi ihmisessä.
Siltä kannalta ajatellen, että "oikopolkuja ei ole" perille menoon nahkakapselissaan itsensä kanssa tässä ajassa, kannaway tuotteitten tehokkaasti tuoma homeostaasin kaltainen (placebo-vaikutus tai ei ) tila on sellaisia varten, jotka eivät tuotteita jatkuvasti tarvitse, koska tarve on vakavin harha illuusiossa, missä elämme. Ehdottomasti Tärkeintä ihmisyydessä tänä aikana ovat sisäisenä työnä tehtävät tunnevapautus ja traumakäsittelytyö ja sen jälkeen tai mukana alkava parantava henkilökohtainen ulottuvuustyöskentely.
Vaihtoehtoisina keinoina elimistössä olemassa olevan endokannabinoidijärjestelmän käynnistelemiseen voi olla ainakin kala, saksanpähkinät, omega 3-pitoiset camelinan, pellavan ja chiasiemenöljyt, mm. ecolomega kalayöljy, mustapippuri, oregano, kaneli ja kurkumiini, niistä, mitä olen henkilökohtaisesti kokeillut, Kossilan suosituksista loput.
Yleiskatsaus hampunsiementen ravitsemusksellisuudesta
https://natureclaim.com/nutrition/info/hemp-seed/
Tieteellinen nimi: Cannabis sativa
Järjestys: Rosales
Suku: Rosas:
Perhe: Cannabaceae
Lyhyesti sanottuna hampun siemenillä on (DV on päivittäinen
arvo):
Tiamiini (1,28 mg |
107% DV).
niasiinia (9,20 mg |
58 % DV)
B6-vitamiinia (0,60 mg |
35 % DV)
folaattia (110,00 mg |
28 % DV)
rauta (7,95 mg |
44 % DV)
magnesium (700,00 mg |
167 % DV)
fosfori (1650,00 mg |
132 % DV)
kalium (1200,00 mg |
26 % DV)
sinkki (9,90 mg |
90 % DV)
kupari (1,60 mg |
178 % DV)
mangaani (7,60 mg |
330 % DV)
Hampunsiemenet (Cannabis sativa) ovat pieniä ja ruskeita
siemeniä, joista voidaan valmistaa monenlaisia tuotteita. Kuorittu hamppu
-siemenissä ei ole siemenkuorta. Hampunsiemenet eivät sisällä kannabidiolia
(CBD), tetrahydrokannabinolia tai kannabidiolia (THC) tai muita kannabinoideja.
Sen sijaan siemenissä on runsaasti proteiinia, tiamiinia, magnesiumia,
fosforia ja sinkkiä, kuparia ja mangaania.
Hampunsiemenet ovat runsas proteiinin lähde (63 %
päivittäisestä arvosta [DV]), joka sisältää suuria määriä lähes kaikkia
välttämättömiä aminohappoja.
Vitamiinit ja tiamiini (107 % DV), auttavat sydämen
toiminnassa, energian luomisessa ja henkisen ja emotionaalisen toimintakyvyn
ylläpitämisessä.
Niasiini (58 % DV) ja B6-vitamiini (35 % DV)
ovat tärkeitä aineenvaihdunnan ja energian kannalta. B-vitamiini, folaatti
(28 % DV), mahdollistaa sikiöiden terveen kehityksen. Magnesium (167
% DV) vähentää väsymystä ja tukee lihaksia, luita, hampaita, hermostoa ja
mielenterveyttä. Fosfori (132 % DV) edistää kehon solujen normaalia
toimintaa, energian luomiseen sekä luuston ja hampaiden terveyteen. Sinkki
(90 % DV) on välttämätön ravintoaine normaalille kehitykselle ja elimistölle
immuunisolujen toimintaan. Rauta (44 % DV) tukee hapen tuotantoa
elimistössä. Kupari (178 % DV) suojaa soluja. vahingollisilta vapailta
radikaaleilta. Kupari mineraalina on myös välttämätön energian luomiselle
kehossa, immuunijärjestelmässä ja hermojärjestelmässä. https://ods.od.nih.gov/factsheets/list-VitaminsMinerals/
Mangaani (330
% DV) voi suojata kehon soluja vaurioilta ja on tärkeä terveille luille,
sidekudokselle ja lihaksille kudosten ja energian luomisen kannalta. Kalium
(26 % DV) auttaa säätelemään sydämen sykettä ja ylläpitämään lihasten ja
hermojen toimintaa.
Hampunsiemenet sisältävät myös ravintokuitua (14 %
DV), joka lievittää ummetusta ja edistää suoliston terveyttä. Hampunsiemeniä
voidaan syödä raakana, jauhaa hamppujauhoksi, itää tai tehdä kuivattua
itujauhetta lihasten ja hermojen toiminnassa.
Merkintä ”-” tarkoittaa riittämättömiä tietoja.
% Päivittäiset arvot perustuvat 2000 kalorin ruokavalioon
tai viittaavat tietyn elinvaiheen ruokavalion viiteannoksiin.
Viite(t):
U.S.
Department of Agriculture, Agricultural Research Service. FoodData Central,
Current Release.
https://ods.od.nih.gov/factsheets/list-VitaminsMinerals/
Yleiskatsaus Cannabidiolumiin
Cannabis sativa -kasvin uutteet sisältävät kannabidiolia
(tunnetaan myös nimellä CBD), joka on kannabinoidi, pitoisuuksina, jotka ovat
40 % tai enemmän [Bergamaschi et al. 2011]. (Cannabis indica on Cannabis
sativan synonyymi.) CBD:tä käytetään ja markkinoidaan yleisesti CBD-öljynä.
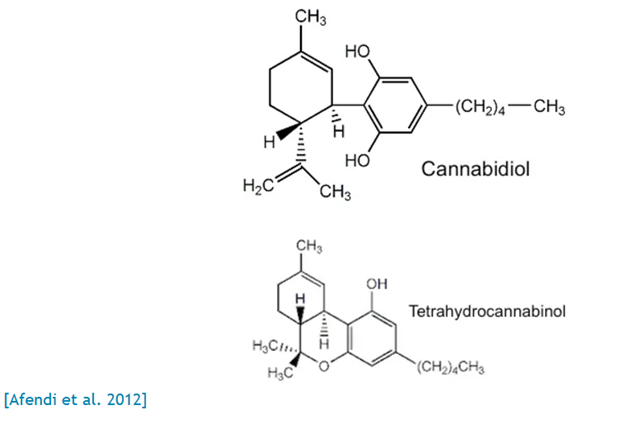
Toisin kuin tetrahydrokannabinolilla (THC), CBD:llä ei ole psykoaktiivisia
ominaisuuksia. CBD ja THC:llä on samanlainen molekyylipaino, mutta erilainen
rakenne (ks. yhdisteet). Vuonna 2018 Yhdysvaltain elintarvike- ja Drug Administration
(FDA) hyväksyi kannabiksesta saatavan erittäin puhtaan kannabidioliuutteen
epilepsian hoitoon. Saman määrän CBD:tä ja THC:tä sisältävä uute on myös
hyväksytty käytettäväksi useissa Euroopan maissa multippeliskleroosin (MS)
oireiden hoitoon. Useimmissa tutkimuksissa on tutkittu tehoa
CBD/THC-yhdistelmien vaikutusta eri terveysongelmien hoitoon. Siksi tarvitaan
lisää tutkimusta, jotta voidaan tutkia CBD:n lääkinnällisiä ominaisuuksia
yksinään. CBD:tä markkinoidaan tällä hetkellä ihmelääkkeenä (tai yleislääkkeenä);
Useimmilla väitteillä on kuitenkin vain vähän tai ei lainkaan tukevaa näyttöä,
kuten kivunhoidon osalta. Mitä tulee hampun ravintoarvosta, katso
hampunsiemenet. Kalifornian osavaltion mukaan kannabiksen (marihuanan) savu
aiheuttaa syöpää ja on kehityshäiriö / lisääntymismyrkky [Proposition 65
-varoitus].
Todisteet
Vahva:
CBD
yksinään, joka on FDA:n hyväksymä:
© Epilepsia
lapsilla [2-11]
© Sisältää:
Dravetin oireyhtymä ja Lennox-Gastautin oireyhtymä.
2. Alvarez
Bravo G, Yusta Izquierdo A. Dravetin oireyhtymän aikuisten motorinen fenotyyppi
liittyy mutaatioon, joka liittyy STXBP1-geeniin ja reagoi hyvin
kannabidiolihoitoon. Seizure. 2018 Aug;60:68-70. doi:
10.1016/j.seizure.2018.06.010.
Epub 2018 Jun 13. PubMed PMID: 29929108.
Hyvä:
Pelkkä
CBD:
* Torjuu
kannabiksen ja tetrahydrokannabinolin (THC) myrkytyksen ja psykoosin
vaikutuksia [12-28].
CBD/THC-yhdistelmät:
*
Kannabisriippuvuus ja vieroitus [29-34].
*
Multippeliskleroosipotilaat (MS) [35-77]
CBD/THC-yhdistelmät:
*
Kannabisriippuvuus ja vieroitus [29-34].
*
Multippeliskleroosipotilaat (MS) [35-77]
Lupaava:
CBD
yksinään:
”
Ahdistuneisuushäiriöt [78-80]
CBD/THC-yhdistelmät:
” Allodynia
[81-83]
” Syöpään
liittyvä kipu [84-86]
Ristiriitainen
(epäselvä):
CBD
yksinään:
”
Skitsofrenia [87-90]
Rajallinen
näyttö:
CBD
yksin:
*
Kannabisriippuvuus ja vieroitus [91].
* Krooninen
kipu munuaisensiirtopotilailla [92]
*
Dysautonominen oireyhtymä ihmisen papilloomaviruksen (HPV) rokotuksen jälkeen
[93].
*
Epidermolysis Bullosa lapsilla, paikallinen CBD-öljy [94].
* Kuumeinen
infektioon liittyvä epilepsiaoireyhtymä (FIRES) [95].
* Graft-Versus-Host-tauti (GVHD) [96].
*
Pahanlaatuiset migraatiopartiokohtaukset [97].
*
Parkinsonin tauti [98]
*
Posttraumaattinen stressihäiriö (PTSD) lapsilla [99].
* Lopullinen
tupakointi (tupakoinnin lopettaminen) [100]
* REM-unen
käyttäytymishäiriö (RBD) Parkinsonin tautia sairastavilla potilailla [101].
*
Sosiaalinen ahdistuneisuushäiriö (SAD) [102-103].
* Kasvaimet,
synteettinen CBD [104]
* Tyypin 2
diabetes, tetrahydrokannabivarin (THCV) voi olla tehokkaampi [105].
CBD/THC-yhdistelmät:
ADHD [106]
*
Niveltulehdus [107]
* Syöpään
liittyvä anoreksia-kacheksia-oireyhtymä [108]
* Keskusneuropaattinen
kipu Brachial Plexus Avulsion [109]
*
Kemoterapian aiheuttama pahoinvointi ja oksentelu [110].
*
Kemoterapian aiheuttama neuropaattinen kipu [111].
* Krooninen
kipu [112]
© Epilepsia
lapsilla [113]
* Kivulias diabeettinen
perifeerinen neuropatia [114-115].
* Jäykän
henkilön oireyhtymä (SPS) [116].
* Touretten
oireyhtymä (TS) [117].
Ei
näyttöä:
CBD
yksin:
”
Kaksisuuntainen mielialahäiriö [118]
Krooninen
kipu [119]
Crohnin
tauti [120]
Huntingtonin
tauti [121]
Glaukooma
[122]
CBD/THC-yhdistelmät:
”
Huntingtonin tauti [123]
Ei
kliinistä tutkimusta:
” Ja kaikki
muut tilat.
Sivuvaikutukset
” Vähentynyt
ruokahalu
” Ripuli
”
Tarkkaavaisuuden häiriöt
” Huimaus
”
Uneliaisuus
” Kuiva suu
” Päänsärky
”
Ajoittaiset kuuman olon jaksot
”
Pahoinvointi
” Vältä tai
ota yhteyttä laillistettuun terveydenhuollon ammattilaiseen, jos sinulla on tai
on ollut masennusta, psykoottisia häiriöitä ja skitsofreniaa. CBD voi heikentää
immuunijärjestelmää, eikä sitä tule käyttää, jos sinulla on seuraavia
sairauksia
HIV-infektio.
” Yleisesti
ottaen tutkijat ovat todenneet, että CBD on turvallisempaa kuin
tetrahydrokannabinoli (THC), koska CBD:llä on antipsykoottisia ominaisuuksia ja
se voi torjua THC:n vaikutuksia.
” Vaikka
kannabiksen on yhdistetty aiheuttavan amotivaatio-oireyhtymää (ts.
irrottautumista, puutetta, (toiminnanohjauksen ) puutetta drive and emotions),
CBD:n ottaminen ei parantanut motivaatiota.
” Koska
CBD:tä ja skitsofreniapotilaita koskevia tutkimuksia ei ole riittävästi, CBD
saattaa aiheuttaa enemmän haittaa kuin hyvää tai ei mitään.
* Koska
CBD:tä ja skitsofreniapotilaita koskevia tutkimuksia ei ole riittävästi, CBD
voi aiheuttaa enemmän haittaa kuin hyvää tai ei mitään.
*
Skitsofrenian puhkeaminen voi johtua THC:stä, mutta ei CBD:stä.
* CBD:n ei
ole osoitettu aiheuttavan kromosomivaurioita.
* CBD ei
näytä vaikuttavan suorituskykyyn.
[124-138]
Raskaana
oleva tai imettävä
CBD:tä
sisältävien lisäravinteiden käytöstä raskauden ja imetyksen aikana ei ole
riittävästi tutkimustietoa...
imetyksen
aikana, joten ota yhteyttä luvan omaavaan terveydenhuollon ammattilaiseen ennen
käyttöä tai vältä käyttöä.
CBD:tä ei
kuitenkaan suositella käytettäväksi raskauden ja imetyksen aikana.
Vuorovaikutukset
Suuret:
Sytokromi
P450:n (CYP) muuttamat lääkkeet maksassa.
Alkoholi
Ketamiini
Tetrahydrokannabinoli
(THC)
A-vitamiini
[139-147]
Kohtalainen:
”
Syöpälääkkeet
[139-147]
Potentiaalinen:
CBD:llä EI ole yhteisvaikutuksia Secobarbitalin ja opioidin,
Fentanyylin, kanssa.
[139-147]
Annostus
CBD-öljylisät
eivät ole ”lääkkeitä”, eikä parhaita annoksia ole vahvistettu perusteellisesti.
Varmista, että noudatat tuotteen erityisohjeita ja ota etiketissä annettujen ohjeiden
mukaisesti tai ota yhteyttä luvan omaavaan terveydenhuollon ammattilaiseen,
lääkärin kanssa ennen käyttöä.
REFERENSSIT
https://natureclaim.com/medicine/info/cannabidiolum/#references
Kannabigerolin CBG ja sen synteettisten johdannaisten farmakologiset näkökohdat ja biologiset vaikutukset
https://pmc.ncbi.nlm.nih.gov/articles/PMC9666035/
Kannabigeroli (CBG) on Cannabis sativa -kasvin kannabinoidi,
jolla ei ole psykotomimeettisiä vaikutuksia. Sen esiaste on sen hapan
muoto, kannabigerolihappo (CBGA), joka puolestaan on kannabidioli
(CBD) ja Δ9-tetrahydrokannabinoli (THC) -yhdisteiden biosynteettinen
esiaste. CBGA:n dekarboksylointi johtaa neutraalin kannabinoidin CBG:n
muodostumiseen lämmön katalysoiman kemiallisen reaktion kautta. CBG:hen
kohdistuvan kasvavan kiinnostuksen perusteella ja tätä kasvikannabinoidia
koskevan tieteellisen tiedon korostamiseksi keskityimme tämän artikkelin
sisällössä sen farmakokineettisiin ja farmakodynaamisiin ominaisuuksiin sekä
sen tärkeimpiin farmakologisiin vaikutuksiin. CBG metaboloituu maksassa
CYP2J2-entsyymin avulla hydroksyyli- ja di-oksituotteiksi. CBG:tä pidetään
CB1-reseptorin (R) ja CB2R:n osittaisena agonistina sekä endokannabinoidien
signaloinnin säätelijänä. CBG:n mahdollisia farmakologisia kohteita ovat
transienttireseptoripotentiaalikanavat (TRP-kanavat),
syklo-oksygenaasientsyymit (COX-1 ja COX-2), kannabinoidi-, 5-HT1A- ja
alfa-2-reseptorit. Prekliiniset havainnot osoittavat, että CBG alentaa
silmänpainetta, sillä on antioksidanttisia, anti-inflammatorisia ja
kasvaimia ehkäiseviä vaikutuksia ja sillä on ahdistusta vähentäviä,
neuroprotektiivisia, dermatologisia ja ruokahalua stimuloivia vaikutuksia. Useat
havainnot viittaavat siihen, että CBG:tä koskevaa tutkimusta on syytä syventää,
koska sitä voitaisiin käyttää yksin tai yhdessä uusien terapeuttisten
lähestymistapojen löytämiseksi useisiin sairauksiin.
1. Johdanto
Cannabis sativa L.:n (fam. Cannabaceae; C. sativa)
lisääntynyt terapeuttinen potentiaali ja sen kemiallisten ainesosien
farmakologia edellyttävät syvällisempää ymmärrystä sen muiden ainesosien kuin
tunnetumpien fytokannabinoidien Δ9-tetrahydrokannabinolin (THC) ja
kannabidiolin (CBD) osalta (kuva 1). C. sativan tärkeimmän psykoaktiivisen
ainesosan THC:n eristämisen jälkeen [1, 2] tästä kasvista on löydetty yli
100 fytokannabinoidia, joista yksi on kannabigeroli (CBG)
[3].
Muutama vuosi THC:n tunnistamisen jälkeen (kuva 1) in vivo
-tutkimukset osoittivat, että fytokannabinoidi CBG ei ole psykotomimeettinen
kuten tunnetumpi fytokannabinoidi THC [4, 5]. Sitä on kuitenkin laiminlyöty
ja varjostettu THC:n rinnalla vuosien ajan sen pienemmän pitoisuuden vuoksi
ja paradoksaalisesti luultavasti sen psykotomimeettisen aktiivisuuden
puuttumisen vuoksi. CBG on C. sativa -kasvin terpeenofenolinen
fytokannabinoidin esiaste sekä THC:lle että CBD:lle [6]. CBG:tä ei esiinny
ainoastaan tässä kasvissa; sen lisäksi, että se on löydetty C. sativasta, sitä
on löydetty myös Helichrysum umbraculigerum -kasvin uutteen fytokemiallisesta
profiilista, jota pidetään runsaimpana CBG:n lähteenä [7] (kuva 1).
Kasveissa kannabinoidit THC ja CBD syntetisoidaan happamassa
(karboksyloituneessa) muodossa, nimittäin kannabigerolihapossa (CBGA) (kuva 1).
CBGA käy läpi dekarboksylaatioprosessin, joka riippuu eri tekijöistä,
erityisesti tämän prosessin nopeus liittyy lämpötilan nousuun (kuva 1).
Dekarboksylaatio, joka aiheuttaa CBG:n muodostumisen, johtuu yksinkertaisesta
kemiallisesta reaktiosta, jota lämpö katalysoi ja joka tapahtuu
huoneenlämmössä, mutta paljon hitaammin [8]. Tätä kannabinoidien välituotetta
ei esiinny kannabiksessa merkittävinä pitoisuuksina, vaan se esiintyy yleensä
pienenä yhdisteenä suhteessa [9, 10]. Kuten THC:n ja CBD:n kohdalla, kasvi
syntetisoi ensisijaisesti CBGA:ta; tämä kannabinoidin hapan muoto on termisesti
epästabiili, ja se voi dekarboksyloitua, kun se altistuu valolle tai
kuumuudelle tupakoinnin, paistamisen tai takaisinvirtauksen kautta [11]. Tässä
artikkelissa tuodaan esiin CBG:tä koskevaa nykyistä tieteellistä tietoa
keskittyen sen farmakokineettisiin ja farmakodynaamisiin ominaisuuksiin ja sen
tärkeimpiin farmakologisiin vaikutuksiin sekä CBG:stä peräisin olevien
yhdisteiden farmakologisiin vaikutuksiin.
3.1. Anti-inflammatoriset ja antioksidanttiset
vaikutukset
Endokannabinoidijärjestelmä moduloi homeostaattisia
prosesseja, kuten ruoansulatuskanavan motiliteettia, nälkää, kivun
havaitsemista ja immuniteettia [40]. Anti-inflammatorisia ja
antioksidanttisia vaikutuksia tutkittiin pääasiassa prekliinisen tutkimuksen
avulla. Koe-eläintutkimuksissa kannabinoideilla on osoitettu olevan
anti-inflammatorisia vaikutuksia, ja alaryhmäanalyysi osoitti, että
kokeellisessa paksusuolitulehduksessa CBG aiheutti suurimman
myeloperoksidaasiaktiivisuuden vähenemisen ja vaikutuksen koon (SMD -6,20;
95 % CI, -9,90-2,50), ja näiden vaikutusten aikaansaamisessa seurasi
synteettinen CB1-agonisti arakidonyyli-2-kloorietyyliamidi (ACEA) [41].
Antitumoraalinen aktiivisuus
CBG:n vaikutuksia tutkittiin useisiin kasvainsolulinjoihin.
CBG:n antitumoraalista aktiivisuutta ihmisen suun epitelioidisia
karsinoomasoluja vastaan on tutkittu. Näissä in vitro -kokeissa CBG osoitti
antitumoraalista ominaisuutta ihon melanoomasoluja vastaan, ja sillä oli
merkittävä aktiivisuus (IC50 = 31,30 μM) in vitro MTT (3-(4,
5-Dimelhyllhiazol-2-yl)-2, S-difenyyli-2 H-tetra-zoliumbromidi)
-mikroviljelytestissä [49]. Samat kirjoittajat havaitsivat, että CBG esti
suun epidermikarsinooman solulinjojen kasvua, jolloin IC50 oli 31 μM
MMT-määrityksessä ja 77 μM sulforhodamiini B -proteiinimäärityksessä. Näissä
kokeissa CBG:llä oli vähiten sytotoksinen vaikutus hiiren NIH 3T3-soluihin
ja se oli tehokkaampi kuin 5-fluorourasiili [50]. CBG:n havaittiin olevan
tehokas rintasyöpää vastaan ihmisen MDA-MB-231-solulinjassa [51] ja estävän
hyperproliferoivan ihmisen keratinosyyttisolulinjan proliferaatiota [52].
Lisäksi, kuten edellä todettiin, CBG kykenee vähentämään kokeellista
suolistotulehdusta, mikä saattaa olla tärkeää, kun otetaan huomioon paksusuolen
ja peräsuolen syövän riski, joka on huomattavasti suurempi haavaista
paksusuolen tulehdusta sairastavilla potilailla [53]. Tästä näkökulmasta
arvioitiin CBG:n vaikutuksia CRC-solujen kasvuun ja sen mahdollista
ennaltaehkäisevää vaikutusta paksusuolisyövän atsoksimetaanimallissa sekä sen
mahdollista terapeuttista vaikutusta paksusuolisyövän ksenograft-mallissa.
Tässä kokeellisessa mallissa osoitettiin, että CBG edisti apoptoosia,
stimuloi ROS-tuotantoa, sääteli transkriptiotekijä CCAAT-enhancer-binding
protein homologisen proteiinin (CHOP) mRNA:ta ja hidasti solujen kasvua
CRC-soluissa. CBG:n vaikutukset solujen kasvuun eivät olleet riippuvaisia
TRPA1-, TRPV1- ja TRPV2-kanavien aktivoitumisesta, niitä tehosti lisäksi
CB2R-antagonisti SR144528, ja ne saatiin aikaan myös muilla TRPM8-kanavien
salpaajilla, mutta ei 5-HT1A:n antagonistilla rimonabantilla. CBG:n aktiivisuus
solujen kasvuun ja CHOP-mRNA:n ilmentymiseen väheni TRPM8-solulinjassa. CBG
antagonisoi kemikaalien indusoimien ksenograft-syöpien ja paksusuolen
kasvainten kehittymistä. Samassa kokeellisessa mallissa CBG vaikeutti
kasvaimen etenemistä ja esti CRC-solujen etenemistä [54]. Nämä in vivo
-kokeet osoittavat, että CBG vastustaa CRC-solujen kasvua pääasiassa
stimuloimalla apoptoosia ja estämällä paksusuolen karsinogeneesin kehittymistä.
Lisäksi kirjoittajat ovat ehdottaneet, että TRPM8 on myös ainakin osittain
osallisena CBG:n antitumoraalisessa toiminnassa. CBG:n
kasvainsolulinjojen kasvua estävään vaikutukseen liittyy ROS:n ylituotanto, ja
se näyttää olevan osittain TRPM8:n välittämää. CBG:n ilmeinen turvallisuus ja
kokeelliset tulokset osoittavat, että se voisi olla lupaava CRC:n ehkäisyssä ja
hoidossa.
Glioblastooma on aggressiivinen aivosyöpä, jonka esiintyvyys
kasvaa. On havaittu, että CBG, kuten THC:n kanssa tapahtuu, hidastaa tämän
kasvaimen etenemistä ja estää glioblastoomasolujen invaasiota. Lisäksi CBG
vähentää tehokkaasti hoitoresistenttejä glioblastooman kantasoluja [55].
Nämä havainnot osoittavat, että CBG, jolla on myös analgeettisia,
pahoinvointia vähentäviä ja ruokahalua stimuloivia vaikutuksia, voisi olla
uusi glioblastooman liitännäishoito.
Tulehduksellisiin suolistosairauksiin (IBD) kuuluvat
krooniset uusiutuvat tulehdussairaudet Crohnin tauti (CD) ja haavainen
paksusuolitulehdus. CBG:n vaikutuksia tutkittiin jyrsijöiden kokeellisessa
paksusuolen tulehduksessa, joka aiheutettiin kolonensisäisellä
dinitrobentseenisulfonihapolla (DNBS). CBG:n (1-30 mg/kg) antaminen i.p. ennen
kokeellisen koliitin induktiota tai sen jälkeen paransi merkittävästi
DNBS:n antamisen vaikutuksia paksusuolen painon ja pituuden suhteeseen, jota
käytetään tulehduksen aiheuttaman kudosturvotuksen arviointiin [42]. CBG:n
vaikutuksia suolistotulehdukseen on tutkittu myös arvioimalla
myeloperoksidaasiaktiivisuutta, histologista arviointia ja immunohistokemiaa,
mittaamalla interleukiini- (IL)-1β-, IL-10- ja interferoni (IFN)-γ-tasoja
ELISA-menetelmällä, indusoituvaa typpioksidisyntaasia (iNOS) ja COX-2:ta sekä
CuZn-superoksididismutaasin (SOD) aktiivisuutta. Typpioksidin tuotantoa ja
oksidatiivista stressiä on arvioitu mittaamalla CBG:n vaikutuksia hiiren
makrofageihin ja suoliston epiteelisoluihin. Tulokset osoittivat, että CBG
vähentää paksusuolen painon ja pituuden suhdetta,
myeloperoksidaasiaktiivisuutta ja iNOS-ekspressiota, ja nämä tulokset
liittyivät lisääntyneeseen SOD-aktiivisuuteen ja DNBS:n antamisen aiheuttamien
IL-1β:n, IL-10:n ja IFN-γ:n muutosten normalisoitumiseen. Makrofageissa CBG
aiheutti typpioksidin tuotannon ja iNOS-proteiinin (mutta ei mRNA:n)
ilmentymisen vähenemisen. Mielenkiintoista oli, että CB1R-antagonisti
rimonabantti ei muuttanut CBG:n vaikutuksia typpioksidin muodostumiseen, kun
taas CB2R-antagonisti SR144528 tehosti CBG:n typpioksidin tuotannon estoa.
Kirjoittajien johtopäätösten mukaan nämä kokeet osoittavat, että CBG-hoito
kykenee vähentämään kokeellista koliittia vähentämällä typpioksidin
muodostumista makrofageissa CB2R-aktivoitumisen kautta ja vähentämällä
reaktiivisten happilajien (ROS) tuotantoa suolen epiteelisoluissa [43].
Muut kirjoittajat ovat vahvistaneet, että kannabinoidit
estävät oksidatiivista ja nitrosatiivista stressiä moduloimalla iNOS:n
ilmentymistä ja vähentämällä ROS:n määrää [44, 45] ja että CBG:llä on
E-vitamiiniin verrattavissa oleva antioksidanttinen vaikutus [46].
Vetyperoksidin (H2O2) aiheuttaman oksidatiivisen stressin torjumista
antioksidanttista aktiivisuutta on tutkittu hiiren RAW264.7-makrofageissa,
joita on inkuboitu CBG:llä. Todettiin, että 10 μM CBG:tä esti oksidatiivista
stressiä CB2R-stimulaation jälkeen, koska esikäsittely CB2R-antagonistilla
AM630 antagonisoi CBG:n suojaavat vaikutukset, jotka esiintyivät
H2O2-stimuloiduissa makrofageissa, kun taas CB1R:n osallistuminen näyttää
olevan poissuljettua. CBG:n antioksidanttinen aktiivisuus merkitsee hapettimien
signaalien iNOS:n, nitrotyrosiinin ja PPAR-1:n alaregulaatiota estämällä
IκB-α-fosforylaatiota ja ydintekijä-κB:n (NF-κB) translokaatiota sekä
MAP-kinaasireitin säätelyä. Lisäksi on havaittu, että CBG lisää solujen
antioksidanttista puolustusta moduloimalla SOD-1:n ilmentymistä ja estää
siten solukuolemaa [47]. Tämä osoittaa, että CBG voisi olla hyödyllinen uusi
lähestymistapa hapetusstressiin liittyvien häiriöiden hoidossa. CBG voi
toimia tehokkaasti vapaiden radikaalien kerääjänä ja lisätä solujen
antioksidanttista aktiivisuutta MAPK-kinaasin ja NF-κB:n translokaation
kaltaisten reittien moduloinnin kautta ja torjua solukuolemaa.
Koska tulehduksella ja oksidatiivisella stressillä on
myös keskeinen rooli hermoston rappeutumisessa, on tutkittu, voiko CBG:llä
olla neuroprotektiivisia vaikutuksia, jotka torjuvat tulehdusta ja
oksidatiivista stressiä ja siten suojaavat hermosolujen menetystä vastaan. On arvioitu
CBG:n kykyä puolustaa neuroblastoma selkäydin (NSC)-34:n liikehermosoluja
lipopolysakkaridilla (LPS) stimuloiduissa RAW264.7-makrofageissa
aikaansaadulta toksisuudelta.
In vitro MTT [3-(4, 5-dimetyyliditiatsol-2-yyli)-2,
5-difenyyli-2H-tetratsoliumbromidi)] -määrityksellä (solujen metabolisen
aktiivisuuden mittaamiseksi solujen elinkelpoisuuden, proliferaation ja
sytotoksisuuden indikaattorina) havaittiin, että CBG (1-20 μM) vähensi
LPS-stimuloitujen makrofagien aiheuttamaa solujen elinkelpoisuuden
menetystä NSC-34-soluissa. Näissä kokeissa CBG:n esikäsittely vähensi
apoptoosia, mikä ilmeni kaspaasi 3:n aktivaation ja ydinkoodatun proteiinin
Baxin ilmentymisen vähenemisenä, kun taas anti-apoptoottisen proteiinin Bcl-2:n
ilmentyminen oli enemmän koholla. Lisäksi CBG-esikäsittely vähensi
tulehdusta, kuten osoitti immunosytokemiallisesti arvioitujen IL-1β-,
tuumorinekroositekijä-α (TNF)-α-, IFN-Υ- ja PPAR-proteiinipitoisuuksien
väheneminen, mutta myös oksidatiivinen stressi NSC-34-soluissa, joita
käsiteltiin LPS-stimuloidun RAW264.7:n väliaineella. Nämä kokeet viittaavat
siihen, että CBG voi olla potentiaalinen hoito, jota voidaan käyttää
neuroinflammaatiota ja oksidatiivista stressiä vastaan [48].
3.3. Neuroprotektiiviset vaikutukset
CBG kannabiksesta peräisin olevana kemikaalina, joka
ei aiheuta psykotomimeettisiä vaikutuksia, on mielenkiintoinen
potentiaalisena uutena lääkkeenä keskushermoston (CNS) patologioissa.
CBG:n ja CBD:n neuroprotektiivisia vaikutuksia on verrattu
kokeissa, joissa simuloitiin oksidatiivista stressiä ja neurotoksisuutta
sellaisina kuin ne esiintyvät neurologisissa patologioissa rotilla. CBG:llä
ja CBD:llä oli antioksidanttinen vaikutus vetyperoksidille altistuneissa
astrosyyteissä ja ne palauttivat serotoniinipitoisuuden aivokuoressa [56].
CBG:n vaikutuksia on tutkittu myös ihmisen aivojen
mikrovaskulaarisiin endoteelisoluihin (HBMEC), perisyyteihin ja
astrosyytteihin, jotka muodostavat veri-aivoesteen (BBB) iskeemisissä
olosuhteissa. Tämän kokeellisen mallin avulla on osoitettu, että 10 μM CBG:tä
vähensi IL-6:n, laktaattidehydrogenaasin ja DNA-vaurioproteiinien tasoja
astrosyyteissä [57].
CBG:n suojaavia vaikutuksia on tutkittu kahdessa
3-nitropropionaatilla (3NP) indusoidun Huntingtonin taudin (HD) in vivo
-mallissa. CBG, jota annettiin hiirille päivittäisinä neljänä i.p.-injektiona
(10 mg/kg), paransi motorisia puutteita, säilytti striatumin neuronit,
vähensi mikroglioosia ja vähensi 3NP:n indusoimia tulehdusmerkkiaineita
3NP:n myrkyllisyyttä vastaan sekä paransi antioksidanttista aktiivisuutta.
CBG tuotti myös merkittävää elpymistä heikentyneessä
rotarod-suorituskyvyssä. Lisäksi HD array -analyysin avulla oli ilmeistä, että
CBG käänsi normaaliksi joukon tähän patologiaan liittyviä geenejä [58].
Synteettinen analoginen kannabigerolikvinoni VCE-003
(kuva 3), joka on saatu hapettumismuutoksella yhdisteen resorsinoliosassa,
on tunnistettu tulehdusta ehkäiseväksi aineeksi. VCE-003 vähensi
eksitotoksisuuden vaikutuksia hermosoluihin, aktivoi
PPARγ-transkriptioaktiivisuutta ja esti tulehdusta edistävien aineiden
vapautumista kokeellisessa mallissa, jolle on ominaista mikrogliasolujen
stimulointi lipopolysakkaridilla (LPS). Samassa koesarjassa kirjoittajat
havaitsivat, että VCE-003 paransi oireita multippeliskleroosin (MS) mallissa,
jota edusti Theilerin hiiren enkefalomyeliittiviruksen (TMEV) infektio [59].
MS-tauti on krooninen tulehduksellinen demyelinoiva
keskushermoston sairaus, jota pidetään pääasiassa T-solujen välittämänä
autoimmuunisairautena, ja neuroinflammaatio on olennainen osa tämän taudin
patofysiologiaa [60]. On osoitettu, että VCE-003, vähentää
neuroinflammatiota ja motorista puutosta viruksen T-soluissa ja makrofageissa,
ja sen tehokkuutta MS-taudin autoimmuunimallissa on tutkittu. Proliferaatiota,
solusykliä ja aktivaatiomarkkereiden ilmentymistä arvioitiin fluoresenssiaktivoidulla
solulajitteluanalyysillä ihmisen primaarisissa T-soluissa, ja sytokiinien ja
kemokiinien muodostumista kvantifioitiin. Samassa tutkimuksessa tutkittiin
transkriptiota käyttämällä Jurkat- ja RAW264.7-soluja, jotta voitiin arvioida
VCE-003:n aktiivisuutta IL-17:n aiheuttamaan makrofagien polarisaatioon
M1-fenotyypin aktivoimiseksi. Kokeellinen autoimmuuni enkefalomyeliitti (EAE)
indusoitiin myeliini-oligodendrosyyttiglykoproteiinin (MOG35-55)
immunisoinnilla ja selkäydinvaurio todettiin immunohistokemiallisesti. Tulokset
osoittivat, että immunisoinnin jälkeinen i.p. VCE-003:n (5 mg/kg) anto 21
peräkkäisenä päivänä esti CD3/CD28:n stimuloimia proliferatiivisia vaikutuksia,
solusyklin etenemistä ja IL-2Ra:n ja ICAM-1:n induktiota ihmisen T-soluissa.
VCE-003 esti myös Th1/Th17-sytokiinien ja kemokiinien muodostumista hiiren
T-soluissa. Tämä vaikutus liittyi IL-2-, IL-17- ja TNF-α-promoottorien
transkription vähenemiseen CD3/CD28:n indusoimana. Lisäksi VCE-003 ja
CB2-agonisti JWH-133 heikensivät IL-17:n aiheuttamaa makrofagien
pro-inflammatorista polarisaatiota. Toinen VCE-003:n vaikutus oli LPS:n
stimuloiman iNOS-ekspression estäminen. VCE-003 paransi hiirten EAE:n
neurologista profiilia ja ankaruutta CB2- ja PPARc-reseptorien stimulaation
avulla. Lopuksi näissä kokeissa havaittiin soluinfiltraattien vähenemistä, mikä
liittyi mikroglia-aktivaation vähenemiseen, myeliinin rakenteelliseen
säilymiseen ja aksonien suojaamiseen. Näin ollen VCE-003:n potentiaalinen rooli
terapeuttisena yhdisteenä, jota voidaan käyttää immuunisairauksissa, joille on
ominaista tulehdus [61].
3.4. Ahdistusta vähentävät vaikutukset
Endokannabinoidien on osoitettu moduloivan ruokinta- ja
tunnekäyttäytymistä [67, 68]. CBG toimii 5-HT1A-antagonistina, kuten on
osoitettu in vitro [30] ja in vivo -kokeissa [69]. Tästä syystä on ehdotettu,
että se voi olla vastuussa kannabiksen ahdistusta vähentävistä vaikutuksista
[70]. Käsitys siitä, että CBG käyttäytyy 5-HT1A:n antagonistina, on kuitenkin
ristiriidassa sen oletettujen anksiolyyttisten vaikutusten kanssa, koska
agonisti - tai osittainen agonisti - tuottaisi todennäköisemmin anksiolyyttisiä
vaikutuksia. Näitä näkökohtia tutkittiin vertaamalla akuutin ja kroonisen (14
päivää) i.p. CBG: n (2,5 mg / kg) vaikutuksia THC: n (2,5 mg / kg) ja CBD: n
(2,5 mg / kg) kroonisen i.p. antamisen vaikutuksiin avoimessa, valaistussa
laatikossa kulutettuun aikaan ahdistuneisuutta muistuttavan käyttäytymisen
valo-pimeä (LD) upotusmallissa ja sakariini-hedonisia reaktioita makuaistin
käsittelyn makuaistin reaktiivisuuskokeessa rotilla. Tulokset osoittivat, että
THC aiheutti akuutisti anksiogeenisen kaltaista käyttäytymistä LD-
upotuskokeessa, jota ei tehostettu kroonisella annostelulla. THC lisäsi vain
ohimenevästi ensimmäisenä antopäivänä sakariinin maistuvuutta
makureaktiivisuuskokeessa. Sekä CBD että CBG eivät muuttaneet ahdistuksen
kaltaista vastetta, mutta CBG aiheutti sakariinin maistuvuuden lievän
lisääntymisen vain ensimmäisenä antopäivänä. Nämä tulokset eivät pystyneet
vahvistamaan CBG:n ahdistusta vähentäviä vaikutuksia rotilla, koska ne eivät
osoittaneet CBG:n anksiolyyttistä vaikutusta [71]. Toisin kuin näissä
tuloksissa, muissa kokeissa on havaittu, että i.p. CBG:n antaminen hiirille
annoksella 10 mg/kg lisäsi avoimen kenttäkokeen keskimmäisessä kvadrantissa
kulutettua aikaa, mikä viittaa mahdollisiin anksiolyyttisiin vaikutuksiin.
Samassa koeryhmässä CBG:n i.p. antaminen annoksella 3 mg/kg tuotti myös
kevyen anti-nosiseptiivisen vaikutuksen [72].
3.5. Pahoinvointia ehkäisevät vaikutukset
CBG näyttää vaikuttavan THC:n antiemeettisiin
ominaisuuksiin. CBG:n antagonismi CB1R- ja 5-HT1A-reseptoreihin [30] kumoaa
pienen annoksen CBD:n antiemeettisen vaikutuksen, luultavasti siksi, että se
johtuu vaikutuksesta 5-HT1A-reseptoritasolla [64]. On myös arvioitu CBG:n
potentiaalia antagonisoida 5-HT1A-reseptorin 8-OH-DPAT-antagonistin
antieettistä vaikutusta [73]. Suurempien CBD- ja CBG-annosten emeettiset
vaikutusominaisuudet ovat saattaneet osallistua vakavan pahoinvoinnin ja
oksentelun tuottamiseen kannabinoidihyperemeesi-oireyhtymän ilmetessä [74].
Kokeissa on tutkittu ja arvioitu CBG:n mahdollisia vaikutuksia joko
pahoinvoinnin säätelyyn rotilla tai oksenteluun Suncus murinuksella. Kaksi
koetta suoritettiin; kokeessa 1 rotat saivat i.p. CBG:tä (0,0, 1, 5 ja 10
mg/kg) 15 minuuttia ennen kuin ne saivat i.p. yhdistettä tai CBD:tä (5 mg/kg;
koe 1a) tai i.p. yhdistettä tai 8-OH-DPAT:a (0,01 mg/kg; koe 1b). 30 minuutin
kuluttua kaikkia rottia käsiteltiin i.p. 0.1% sakariiniliuoksen ja LiCl: n (20
ml / kg 0.15 M) yhdistelmällä. Seitsemänkymmentäkaksi tuntia myöhemmin
eläimille tehtiin sakariinin makureaktio, jotta voitiin tarkkailla vaikutuksia
ehdollistettujen aukkoreaktioiden (pahoinvoinnin kokeellinen malli) ja
ehdollistetun sakariinin välttämisen perustamiseen. Kokeessa 2 S. murinus
käsiteltiin i.p. CBG:llä (5 mg/kg) tai kantaja-aineella 15 minuuttia ennen
CBD:tä (5 mg/kg) tai kantajaainetta ja 30 minuuttia myöhemmin i.p. LiCl:llä (60
ml/kg 0,15 M) oksenteluepisodien määrän arvioimiseksi. CBD esti ehdollistetun
aukkoisuuden rotilla ja oksentelun shrewsilla, ja nämä vaikutukset
antagonisoitiin esikäsittelyllä kaikilla CBG-annoksilla. CBG myös antagonisoi
8-OH-DPAT:n pahoinvoinnin vastaiset vaikutukset. Nämä tulokset osoittavat, että
CBG: n ja CBD: n kohtuullisten annosten injektio voi olla vastakkainen
toisiinsa nähden 5-HT1A-reseptoritasolla, mikä häiritsee pahoinvoinnin ja
oksentelun modulointia. Nämä havainnot viittaavat siihen, että CBG:tä
voitaisiin käyttää sen mahdollisten vuorovaikutusten vuoksi CBD:n kanssa,
koska sen vaikutus 5-HT1A-reseptorilla on vastakkainen pahoinvoinnissa ja
oksentelussa [69].
3.6. Silmänsisäisen paineen (IOP) alentaminen
Vuonna 1971 havaittiin IOP:n aleneminen ihmisillä poltetun
kannabiksen jälkeen [75]. Myöhemmin eri lajeilla tehdyt havainnot ovat
osoittaneet, että THC:llä on silmänpainetta alentava vaikutus [76].
Cannabinolia (CBN) tai CBG:tä on tutkittu kissoilla antamalla niille
paikallisesti 250, 500 ja 1000 pikogramman annoksia yhtenä pisarana tai
osmoottisten minipumppujen kautta (20 μg/h) yhdeksän päivän ajan. CBN:n
kerta-annoksella oli kohtalainen vaikutus IOP:hen, mutta se vähensi sitä
merkittävästi, jos sitä annettiin kroonisesti. Samoin CBG vähensi IOP:tä, mutta
vaikutuksen suuruus oli suurempi, kun sitä annettiin kroonisesti. Lisäksi CBN
mutta ei CBG aiheutti sivuvaikutuksia, kuten sidekalvon eryteemaa ja
hyperemiaa. CBN:n (20, 40 tai 80 mg/kg) i.p. antamisen jälkeen rotille
havaittiin 8-13 Hz:n polyspiikkipurkauksia sähkökortikogrammissa valppauden ja
unen nopeiden silmänliikejaksojen aikana. Mielenkiintoista on, että
systeemisesti injektoidulla CBG:llä (10, 30 ja 100 mg/kg) ei ollut tätä
vaikutusta. Edellä mainitut tulokset viittaavat siihen, että näiden kannabinoidien
krooninen anto vähentää silmän jännitystä. Kuten kannabiksen ja THC:n
kohdalla, CBN voi kuitenkin aiheuttaa sekä silmätoksisuutta että
neurotoksisuutta. Koska CBG ei aiheuttanut näitä toksisuuksia, on ilmeistä,
että tällä kannabinoidilla saatu silmänpainetta alentava vaikutus voidaan
erottaa sekä kannabikseen liittyvistä haitallisista keskus- että
silmävaikutuksista [77]. Kun CBG:tä annosteltiin kroonisesti yksipuolisesti
kissojen silmiin yhdeksän peräkkäisen päivän ajan osmoottisten minipumppujen
avulla, joista sitä vapautui 1 μl/h, se aiheutti IOP:n laskun samalla tavalla
kuin THC (4-7 mm Hg) samalla tavalla annosteltuna. Sama tutkijaryhmä havaitsi,
että rotilla THC:n, mutta ei CBG:n, perifeerisen annon jälkeen aivokuoren
elektroenkefalogrammissa näkyi polyspiikkipurkauksia heräämisen aikana. Sitten
polyspiikit olivat havaittavissa nopeiden silmänliikkeiden unijaksojen aikana.
Tulokset osoittivat myös, että molemmat kannabinoidit aiheuttivat kaksi- tai
kolminkertaisen lisäyksen vesikalvon ulosvirtaukseen [78]. Koska suurin osa
glaukooman hoidossa käytettävistä lääkkeistä estää kammionesteen vapautumista, CBG
voisi olla lupaava glaukooman vastainen aine, jota voitaisiin käyttää
lääkkeiden kanssa, jotka vaikuttavat tehostamalla kammionesteen ulosvirtausta
sen sijaan, että ne lisäisivät silmänesteen poistumista.
IOP-laskevaa aktiivisuutta tutkittiin rotilla käyttämällä
synteettistä CBG-analogia, kannabigerolidimetyyliheptyyliä (CBG-DMH),
verrattuna epäselektiiviseen CB1R- ja CB2R-agonistiin, WIN55, 212-2. CBG-DMH:n
i.p. anto vähensi IOP:tä 2,5 mg/kg:n annoksilla tai paikallisesti annettuna (1
%-2 %). CBG-DMH:n IOP:tä alentava vaikutus estettiin antamalla i.p. O-1918 (2,5
mg/kg), joka on epänormaalin CBD-herkän kannabinoidireseptorin (CBx)
selektiivinen antagonisti, mutta CB1R-antagonisti AM251 (2,5 mg/kg) tai CB2R-antagonisti
AM630 (2,5 mg/kg) eivät vaikuttaneet siihen. WIN55, 212-2:n samanaikainen
antaminen kynnysarvon alittavalla annoksella IOP:n alentamiseksi (0,25 mg/kg)
yhdessä paikallisen CBG-DMH:n (0,25 %) kanssa lisäsi yksinään käytetyn
yhdisteen IOP:tä alentavaa vaikutusta. Nämä tiedot osoittavat, että CBG:n
analogi vähentää IOP:tä normotensiivisissä rottien silmissä riippumatta CB1R-
tai CB2R-osallistumisesta, luultavasti aktivoimalla putatiivisia
kannabinoidireseptoreita. CB1R-agonisti WIN55, 212-2:n ja CBG-DMH:n
samanaikaisen käytön yhteydessä havaittu suurempi IOP:n aleneminen osoittaa
edelleen, että CBG-DMH:n aiheuttamat vaikutukset silmään liittyvät eri
biologisiin kohteisiin kuin CB1R [79]. Yhdessä nämä havainnot osoittavat, että CBG
voi alentaa silmänpaineen alenemista, ja tämä jälkimmäinen tutkimus viittaa
siihen, että synteettinen CBG voi alentaa silmänpaineen alenemista
mekanismeilla, joihin ei liity CB1R- tai CB2R-aktivaatiota. Tämä havainto
viittaa siihen, että on olemassa putatiivisia kannabinoidireseptoreita, jotka
säätelevät kammionesteen ulosvirtausta ja jotka ovat todennäköisesti
lokalisoituneet silmän etuosan kudoksiin.
3.7. Vaikutukset ihoon
CBG:n vaikutuksia keratiini 1:n ja 10:n, involukriinin ja
transglutaminaasi 5:n ilmentymiseen sekä keratiini 10:n geenin DNA-metylaatioon
on tutkittu ihmisen keratinosyyttien (HaCaT) solulinjassa yhdessä
DNA-metylaation ja neljän DNA-metyylitransferaasin (DNMT1, 3a, 3b ja 3L)
ilmentymisen kanssa. Nämä kokeet osoittivat, että CBG aiheutti merkittävän
vähenemisen tutkittujen geenien ilmentymisessä lisäämällä keratiini 10:n geenin
DNA-metylaatiota. Näistä kokeista saadut tiedot saivat kirjoittajat uskomaan,
että CBG käyttäytyy transkription suppressorina, joka kykenee kontrolloimaan
solujen proliferaatiota ja erilaistumista, ja että se on aine, joka on
mahdollisesti hyödyllinen uusissa ihosairauksien terapeuttisissa
lähestymistavoissa [80]. Tältä pohjalta CBG:tä on tutkittu mahdollisena
aknen vastaisena lääkkeenä. Akne on yleinen ihopatologia; sen vakavampi
ilmeneminen voi kuitenkin heikentää syvästi elämänlaatua ja aiheuttaa
sosiaalisen arvostelun vuoksi psykologisia häiriöitä [81]. CBG:n aknen
vastaisia vaikutuksia sebosyyttien elinkelpoisuuteen ja lisääntymiseen
havaittiin MTT- ja CyQUAN-menetelmillä. CBG vähensi merkittävästi solujen
elinkelpoisuutta 24 tunnin hoidon jälkeen, mutta ei 48 tuntia kestäneellä
hoidolla. CBG (10-20 mM) -hoito 24 tunnin ajan vähensi merkittävästi AEA:n
stimuloimaa lipogeneesiä. Nämä tulokset viittaavat siihen, että CBG voi
toimia osittaisena agonistina saman pro-lipogeenisen signaalireitin kautta,
jolla AEA on aktiivinen. CBG tukahdutti LPS:n sebosyyteihin aiheuttamaa
tulehdusta. Edellä esitettyjen kokeiden tulokset fytokannabinoidien
antiproliferatiivisen vaikutuksen mukaan lisäävät hypoteesia, jonka mukaan nämä
yhdisteet voivat olla hyödyllisiä aknen ja muiden tulehdusominaisuuksiin
liittyvien ihopatologioiden, kuten psoriaasin, hoidossa [82].
3.8. Muut vaikutukset
On esitetty, että jotkin C. sativa -peräiset tuotteet
saattavat vaikuttaa myönteisesti alempien virtsateiden oireisiin. THC:n ja CBD:n
tavoin myös CBG kykenee vähentämään virtsarakon supistuvuutta. CBG:llä on
tehty kokeita hiiren ja ihmisen eristetyillä rakoilla. Erityisesti CBG, jonka
pitoisuudet vaihtelivat välillä 10-8-10-4 M, vähensi asetyylikoliinin
aiheuttamia hiiren virtsarakon supistuksia vaikuttamatta
sähkökenttästimulaation aiheuttamiin virtsarakon supistuksiin. Tulokset
osoittivat, että rimonabantti (10-6 M) tai SR144528 (10-7 M), selektiiviset
CB1R- ja CB2R-antagonistit, eivät muuttaneet CBG:n estävää vaikutusta. CBG
esti myös ihmisen virtsarakon asetyylikoliinin aiheuttamia supistuksia, ja
vaikutus oli merkittävä 3 × 10-5 M- ja 10-4 M-pitoisuuksilla. Nämä havainnot
osoittavat, että CBG on lupaavampi yhdiste kuin muut kannabinoidit ja että
se estää virtsarakon supistumista postsynaptisen vaikutuksen kautta.
Kannabinoidireseptorien mahdollista osuutta on oletettu CBG:n CB1R- ja
CB2R-reseptoreihin kohdistuvan osittaisen agonismin ja CBG:n tunnetun vaikutuksen
perusteella endokannabinoidi anandamidin takaisinoton estoon, ja lopuksi siksi,
että endokannabinoidijärjestelmän komponenteilla on merkitystä virtsarakon
toiminnan säätelyssä. Kannabinoidireseptorien osuutta ei kuitenkaan ole
osoitettu [83, 84].
CBG estää verihiutaleiden aggregaatiota ja [14C]5-HT:n
vapautumista. Kokeissa CBG ei estänyt ihmisen tai kanin verihiutaleiden
tetradekanyyliforboliasetaatin (TPA) aiheuttamaa aggregaatiota; se esti
kuitenkin annosriippuvaisesti (10-3-10-5 M) osittain primaarista aggregaatiota
(johtuen aggregaatiota aiheuttavan aineen suorasta vuorovaikutuksesta sen
reseptorin kanssa) ja esti täysin adrenaliinin aiheuttaman sekundaarisen
aggregaation. CBG esti annosriippuvaisesti myös kanin ja ihmisen
verihiutaleiden aggregaatiota, jota adenosiinidifosfaatti stimuloi (CBG:n
IC50-arvo on 2 × 7 × 10-4 M), ja kanin verihiutaleissa verihiutaleita
aktivoivaa tekijää (pitoisuusalue 3 × 10-5 M ja 10-4 M) [85].
CBG:llä ja muilla tärkeimmillä kannabinoideilla, kuten
CBD:llä, CBC:llä, THC:llä ja CBN:llä, havaittiin aktiivisuutta metisilliinille
resistenttejä Staphylococcus aureus -kantoja (MRSA) vastaan. Mikro-organismien
ja kasviperäisten antibakteeristen yhdisteiden välisen ristiresistenssin
harvinainen esiintyminen viittaa siihen, että CBG:tä voitaisiin tutkia
potentiaalisena yhdisteiden lähteenä antibioottiresistenssin torjumiseksi
[86]. CBG osoitti myös aktiivisuutta Streptococcus mutansia vastaan muuttamalla
bakteerien kalvojen ominaisuuksia indusoimalla hyperpolarisaatiota ja
vähentämällä kalvojen juoksevuutta ja aiheuttamalla sen seurauksena kalvon
läpäisevyyden lisääntymistä [87]. Muut kokeet ovat osoittaneet, että CBG on
potentiaalinen aine bakteerien biofilmiä vastaan, joka on keskeinen tekijä
lääkinnällisten laitteiden kontaminaatiossa ja joka edistää ihmisen kroonisten
infektioiden lisääntymistä [88].
C. sativan ruokahalua stimuloivat vaikutukset on pääasiassa
liitetty THC:hen, mutta CBG on myös ruokahalua stimuloiva aine. CBG, jota
annetaan rotille per os annoksena 30-240 mg/kg, lisää ruokahalua ja
ruokailukäyttäytymistä ilman vaikutusta motoriseen aktiivisuuteen [89, 90].
Koska lihaskato, anoreksia ja aineenvaihdunnan häiriöt ovat yleisiä seurauksia
sytotoksisilla lääkkeillä toteutetusta kemoterapiasta, C. sativa -johdannaisia
käytettiin vähentämään näitä vaikutuksia onkologisilla potilailla. Tässä tarkoituksessa
käytettiin eniten kannabisuutteita, jotka sisälsivät merkittäviä määriä THC:tä
tai synteettisiä THC-analogeja. Valitettavasti THC:n psykotomimeettiset
vaikutukset ovat esteenä sen hyödyntämiselle. Tästä syystä CBG:n ruokahalua
stimuloivan vaikutuksen perusteella on arvioitu koe-eläimillä, vähentääkö tämä
kolmen päivän ajan suun kautta annettu kannabinoidi anoreksiaa ja/tai muita
kachektisia oireita, jotka on aiheutettu i.p. annosteltavalla
sytostaatti-sisplatiinilla (6 mg/kg). CBG kykeni vähentämään sisplatiinin
aiheuttamaa anoreksiaa, painonpudotusta ja aineenvaihdunnan häiriöitä [91].
Äskettäin syntetisoitiin kolme uutta CBG-johdannaista
(HUM-223, HUM-233 ja HUM-234) (kuva 4), joilla on anti-inflammatorisia ja
analgeettisia ominaisuuksia. Lisäksi yksi niistä, HUM-234, pysäytti
lihavuuden kehittymisen hiirillä, joita ruokittiin runsaasti rasvaa
sisältävällä ruokaohjelmalla [92].
4. Päätelmät
CBG on
happamassa muodossaan tunnetuimpien kannabiksen johdannaisyhdisteiden eli THC:n
ja CBD:n esiaste. Sen farmakologian tutkiminen osoittaa, että tällä yhdisteellä
on joitakin yhteisiä ominaisuuksia muiden fytokannabinoidien kanssa, mutta
sillä on oma tyypillinen profiilinsa, kuten uudet tutkimukset osoittavat.
Farmakodynaamiset tutkimukset viittaavat vaikutusmekanismiin, johon liittyy
vain osittainen klassisten kannabinoidireseptoreiden aktiivisuus, mikä
osoittaa, että CBG:llä, samoin kuin CBD:llä, on farmakologinen
monikohdevaikutus ja että se on vuorovaikutuksessa useiden
endokannabinoidien ja muiden kuin endokannabinoidien kohteiden kanssa (kuva 3).
Sekä in vivo että in vitro -tutkimukset osoittavat CBG:n useita
farmakologisia vaikutuksia, kuten silmänpaineen alenemista ja dermatologisia,
anti-inflammatorisia, antioksidanttisia, antitumoraalisia ja ahdistusta
lievittäviä vaikutuksia sekä ruokahalua stimuloivia vaikutuksia. CBG:tä
koskeva tutkimus osoittaa myös synteettisten johdannaisten tuotannon kehittymistä.
Synteettisiä analogeja on testattu, ja niillä on ollut myönteisiä vaikutuksia
erityisesti neuroprotektiossa. CBG:llä saadut lupaavat tulokset ja se, että
ilmeisesti ei ole psykotomimeettisiä THC:n kaltaisia vaikutuksia, viittaavat
siihen, että CBG:n tutkimusta on syytä syventää, koska sitä voitaisiin
käyttää yksin tai yhdessä uusien terapeuttisten lähestymistapojen löytämiseksi
useisiin sairauksiin. Nämä vaikutukset on kuitenkin osoitettu vain
prekliinisissä kokeissa, ja kliinistä tutkimusta tarvitaan näiden mahdollisten
vaikutusten vahvistamiseksi ihmisillä.
Yhteenvetona voidaan todeta, että Koillis-Romaniassa viljellystä C. sativa L. -lajista, jonka nimi on KC Dora, uutettiin hamppuöljyä etanolilla huoneenlämmössä, ja liuottimen tyhjiöhaihduttamisen jälkeen saatiin 5,09 prosentin saanto kasviaineesta. Uutetun hamppuöljyn CBD-pitoisuus ja -puhtaus määritettiin flash-kromatografialla ja 1H- ja 13C-NMR:llä. Löysimme tehokkaimmat dekarboksylaatio-olosuhteet CBDA:lle hamppuöljystä (90 °C, 1 tai 2 h), jolloin saadaan CBD:tä runsaasti sisältävää hamppuöljyä ilman bioaktiivisten yhdisteiden merkittävää hajoamista.
Saatu CBD:llä rikastettu hamppuöljy kykeni vähentämään rautaa, puhdistamaan vapaita radikaaleja ja estämään lipidiperoksidaatiota hapettumisolosuhteissa, mikä viittaa siihen, että se voisi suojata hapettumisvaurioilta normaaleissa soluissa. Sitä vastoin CBD:llä rikastettu hamppuöljy indusoi ROS-tuotantoa syöpäsoluissa, mutta tarkkojen mekanismien selvittämiseksi on tehtävä laajempia tutkimuksia. Lisäksi CBD:llä rikastettu hamppuöljy edisti normaalien fibroblastien lisääntymistä, kun CBD:n pitoisuus oli jopa 15 µg/ml, mutta oli sytotoksinen syöpäsoluille. Tietojemme mukaan tämä on ensimmäinen tutkimus, jossa tutkitaan CBD:n tai hamppuöljyn sytotoksisia vaikutuksia osteosarkoomasoluihin, ja tulokset osoittavat, että CBD:llä rikastettu hamppuöljy oli selektiivinen osteosarkoomasoluille ja indusoi apoptoosia annosriippuvaisesti p53- ja ROS-riippumattomilla mekanismeilla.
CBD:llä rikastettu hamppuöljy edisti apoptoosia (solujen itsetuhoisuutta) tutkituissa pahanlaatuisissa solulinjoissa p53:sta riippumattomien mekanismien kautta, mikä on ristiriidassa muiden julkaistujen tietojen kanssa [30]. Koska CBD:n ja hamppuöljyn vaikutukset TP53- ja MDM2-geenien ilmentymiseen ovat antagonistisia, tarvitaan lisää tietoja tämän mekanismin selvittämiseksi eri syöpätyypeissä.
-
https://pmc.ncbi.nlm.nih.gov/articles/PMC7400098/
Teollisuushamppu (Cannabis sativa L.): ravitsemuksellinen laatu ja mahdollinen toimivuus ihmisten terveyden ja ravitsemuksen kannalta.
Abstrakti
Hampunsiemeniä, Cannabis sativa L. -kasvin syötäviä
hedelmiä, pidettiin alun perin teknisen hamppukuituteollisuuden sivutuotteena.
Nykyään, kun C. sativa L. -kasvien, joiden
delta-9-tetrahydrokannabinolipitoisuus (THC) on alle 0,3 % tai 0,2 %
(teollisuushamppu), viljely on aloitettu uudelleen, kiinnostus hampunsiementen
tuotantoon on kasvanut niiden korkean ravintoarvon ja toiminnallisten
ominaisuuksien vuoksi. Tämän katsauksen tavoitteena on tarkastella
hampunsiementen ravitsemuksellisia ja toiminnallisia ominaisuuksia koskevaa
tieteellistä kirjallisuutta. Lisäksi tarkistetaan tieteellistä kirjallisuutta,
joka koskee hampunsiementen ja niiden johdannaisten mahdollista käyttöä
ravintolisänä tulehduksellisten ja kroonisten degeneratiivisten sairauksien
ehkäisyssä ja hoidossa eläinmalleissa ja myös ihmisillä. Työn ensimmäisessä
osassa annamme tietoa tämän kasvin geneettisistä, biokemiallisista ja
lainsäädännöllisistä näkökohdista, jotka ovat mielestämme olennaisia, jotta
voidaan ymmärtää ero "teollisen" ja "huumehampun" välillä.
Katsauksen viimeisessä osassa tarkistetaan myös elintarviketeollisuuden
käyttämää hampunsiementä karjan rehun lisänä ja ainesosana päivittäisten
elintarvikkeiden rikastamisessa tai täydentämisessä. Kaiken kaikkiaan tämän
katsauksen tarkoituksena on kannustaa uusiin ja kattaviin tutkimuksiin
hampunsiementen käyttöönotosta funktionaalisten elintarvikkeiden alalla.
6. Päätelmät
Teollisen hampun (eli C. sativa L. -kasvin lajikkeiden,
joiden THC-pitoisuus on <0,3 tai 0,2 % naaraspuolisen kasvin
lisääntymiskykyisen osan kuivapainosta kukinnan aikaan) viljelyn elpymisen
jälkeen viime vuosikymmeninä on kasvanut kiinnostus tämän kasvin syötäviä
hedelmiä eli hampunsiemeniä kohtaan, joita alun perin pidettiin teknisen
hamppukuituteollisuuden sivutuotteena huolimatta niiden suuresta
ravitsemuksellisesta ja terveydelle hyödyllisestä voimasta, jota on alettu
tutkia suhteellisen äskettäin. Tieteellisen kirjallisuuden analyysi osoitti,
että ravitsemuksellisesti nämä öljykasvien siemenet sisältävät 25-35 prosenttia
lipidejä, joilla on ainutlaatuinen ja täysin tasapainoinen FA-profiili, jolle
on ominaista yli 80 prosenttia PUFA:ta ja jossa EFA:t n-6 LA ja n-3 ALA ovat
täydellisessä suhteessa ihmisten ravitsemukseen ehdotetun mukaisesti. Lisäksi
hampunsiementen saippuoitumaton öljyfraktio sisältää runsaasti tokoferoleja,
joilla on korkea antioksidanttinen aktiivisuus ja jotka ovat välttämättömiä
PUFA:iden suojaamiseksi hapettumiselta, sekä fytosteroleja, kuten
β-sitosterolia. Hampunsiemenet sisältävät myös 20-25 prosenttia
biologisesti arvokkaita, helposti sulavia ja runsaasti välttämättömiä
aminohappoja sisältäviä proteiineja sekä runsaasti makro- ja mikroelementtejä.
Korkean ravintoarvon lisäksi hampunsiemenille on ominaista myös erilaisten
bioaktiivisten yhdisteiden esiintyminen, joihin kuuluu ainutlaatuisia fenoleita
sekä bioaktiivisia peptidejä, joilla on antioksidanttisia, tulehdusta
ehkäiseviä, hermoja suojaavia, verenpainetta alentavia, antiproliferatiivisia
ja hypokolesterolemisia vaikutuksia, joita on arvioitu pääasiassa in vitro
-tutkimuksissa. Hampunsiemenistä ei kuitenkaan täysin puutu joitakin
ravintoarvoja heikentäviä yhdisteitä, jotka voivat vaikuttaa kielteisesti
proteiinien ja kivennäisaineiden sulatukseen ja biologiseen hyötyosuuteen,
ennen kaikkea tI:t ja fytiinihappo.
Koska hampunsiementen ravitsemuksellinen koostumus ja
toiminnalliset ominaisuudet ovat optimaaliset, jotkut tutkijat ovat tutkineet
eläinmallien ja ihmistutkimusten avulla toisaalta hampunsiementen ravintolisän
vaikutuksia terveyteen ja tiettyihin patologisiin tiloihin, ja toisaalta
mahdollisuutta käyttää hampunsiemeniä elintarviketeollisuudessa rehun
lisäaineena, jolla voidaan parantaa eläimistä saatavien elintarvikkeiden
ravitsemuksellista laatua, sekä ainesosana, jolla voidaan rikastaa tai
vahvistaa päivittäisiä elintarvikkeita. Kaiken kaikkiaan eläinmalleilla
tehdyissä tutkimuksissa on tuotu esiin, että hampunsiementen ravintolisän
suojaavista ja suotuisista vaikutuksista erityisesti tulehduksellisiin ja
kroonisiin rappeutumissairauksiin, kuten sydän- ja verisuonitauteihin ja
hermoston rappeutumissairauksiin, on jonkin verran näyttöä, kun taas
ihmisillä tehdyissä tutkimuksissa on havaittu, että hampunsiemenöljyn
nauttiminen ruokavaliosta on vaikuttanut myönteisesti atooppisen dermatiitin
hoitoon, tiettyihin veriparametreihin ja tulehdusreaktioiden modulaatioon.
Tieteellisessä kirjallisuudessa on kuitenkin edelleen vain vähän ja melko
epäselviä artikkeleita, jotka koskevat vain hampunsiemenöljyä, eikä niitä voida
kovin hyvin verrata keskenään, koska niissä käytetään erityyppisiä
koejärjestelyjä sekä erilaisia annoksia, koejaksoja ja lisäravinteiden
antomenetelmiä. Tutkimukset, jotka koskivat hampunsiementen tai niiden
johdannaisten käyttöä elintarviketeollisuudessa, osoittivat, että nämä tuotteet
voivat tehokkaasti parantaa joidenkin eläinperäisten elintarvikkeiden, kuten
munien, maidon ja lihan, FA-profiilia, kun niitä käytetään rehun lisäaineena,
kun taas kun niitä käytetään rikastettujen tai väkevöityjen elintarvikkeiden
ainesosina, rikastettujen/väkevöityjen tuotteiden reologisessa ja
aistinvaraisessa hyväksyttävyydessä tapahtui monia muutoksia, ja useinkaan ne
eivät olleet positiivisia ravitsemuksellisen laadun paranemisesta huolimatta.
Siksi tarvitaan lisätutkimuksia, jotta voidaan laajentaa tutkimusta ja
tietämystä hampunsiementen tai niiden johdannaisten mahdollisesta käytöstä
funktionaalisten elintarvikkeiden kehittämisessä. Erityisesti on tarpeen
ymmärtää, mitkä ovat toimivimmat hampunsiemenen yhdisteet, niiden
molekyylimekanismit ja kohteet, jotta voidaan ymmärtää, mikä on toimivien
yhdisteiden sopivin pitoisuus ja mikä on sopivin väline/matriisi, joka
säilyttää niiden rakenteen ja toimivuuden ruoansulatuskanavassa ja maksimoi
niiden biologisen hyötyosuuden ihmiskehossa. Lisäksi on määriteltävä paras
kompromissi toiminnallisuuden sekä reologisten ja aistittavien ominaisuuksien
välillä ottaen huomioon, että kuluttajat, jotka ovat tietoisia
täydennettyjen/rikastettujen tuotteiden hyödyllisistä vaikutuksista
tavanomaiseen vastineeseen verrattuna, voivat sietää aistittavuuden
jonkinasteista heikkenemistä.
https://pmc.ncbi.nlm.nih.gov/articles/PMC7023045/
Cannabidiolin antioksidatiiviset ja anti-inflammatoriset ominaisuudet
Abstrakti
Cannabidioli (CBD) on yksi Cannabis sativa L:n tärkeimmistä
farmakologisesti aktiivisista fytokannabinoideista. CBD ei ole psykoaktiivinen,
mutta sillä on useita hyödyllisiä farmakologisia vaikutuksia, kuten
tulehdusta ehkäiseviä ja antioksidanttisia ominaisuuksia. CBD:n kemiaa ja
farmakologiaa sekä erilaisia molekyylikohteita, kuten kannabinoidireseptoreita
ja muita endokannabinoidijärjestelmän osia, joiden kanssa se on
vuorovaikutuksessa, on tutkittu laajasti. Lisäksi prekliiniset ja kliiniset
tutkimukset ovat edistäneet ymmärrystä CBD:n terapeuttisesta potentiaalista
monissa sairauksissa, mukaan lukien hapetusstressiin liittyvät sairaudet.
Tässä tarkastelemme CBD:n ja sen synteettisten johdannaisten tärkeimpiä
biologisia vaikutuksia keskittyen CBD:n solu-, antioksidanttisiin ja
anti-inflammatorisiin ominaisuuksiin.
Chelating hakusana:
CBD
vähentää myös reaktiivisten happilajien (ROS) tuotantoa kelatoimalla Fentonin reaktioon osallistuvia
siirtymämetalli-ioneja,
jotka muodostavat erittäin reaktiivisia hydroksyyliradikaaleja [27].
Osoitettiin, että CBD, joka toimii samalla tavalla kuin klassinen
antioksidantti butyylihydroksitolueeni (BHT), estää dihydrorodamiinin
hapettumista Fentonin reaktiossa [28]. Lisäksi CBD:n on havaittu vähentävän
β-amyloidin muodostumista neuroneissa vähentämällä
siirtymämetalli-ionien pitoisuutta [29].
CBD:n epäsuorat antioksidanttiset vaikutukset
Erilaiset
solujen aineenvaihduntajärjestelmät, mukaan lukien endokannabinoidijärjestelmä,
osallistuvat redox-tasapainon säätelyyn. Siten CBD:n toiminta
fytokannabinoidina voi tukea endokannabinoidijärjestelmän biologista toimintaa.
CBD:n on äskettäin osoitettu moduloivan endokannabinoidijärjestelmän toimintaa
lisäämällä anandamidin (AEA) tasoja [5], mikä voi vaikuttaa kannabinoidien
signalointiin, mukaan lukien niiden vuorovaikutus kannabinoidireseptoreihin
[57]. Tiedetään kuitenkin, että esimerkiksi endokannabinoidien aktivoima
peroksisomaalinen proliferaattoriaktivoitu reseptori alfa (PPAR-α) säätelee
suoraan antioksidanttisten entsyymien, kuten superoksididismutaasin,
ilmentymistä vuorovaikutuksessa niiden promoottorialueiden kanssa [58]. Siksi
uskotaan, että CBD:n, kuten endokannabinoidienkin, tärkein antioksidanttinen
vaikutus liittyy sen vaikutukseen reseptoreihin. CBD voi pitoisuudesta riippuen
aktivoida, antagonisoida tai inhiboida kannabinoidireseptoreita (CB1 ja CB2)
sekä ionotrooppisia (TRP) ja ydinsisäisiä (PPAR) reseptoreita (kuva 4)
[52,59,60].
6. Päätelmät
ROS:n
ylituotannosta johtuva oksidatiivinen stressi on keskeinen osa
immuunijärjestelmän vastetta, jolla se torjuu patogeenejä ja käynnistää
kudosten korjaamisen. ROS:n ylituotannosta johtuvilla metabolisilla muutoksilla
on kuitenkin myös monia kielteisiä näkökohtia, ja ne johtavat monien
sairauksien kehittymiseen ja/tai pahenemiseen. Endokannabinoidijärjestelmän,
johon kuuluvat G-proteiinikytkentäiset reseptorit ja niiden endogeeniset
lipidiligandit, uskotaan olevan vastuussa hapetusstressin terapeuttisesta
moduloinnista eri sairauksissa. Tässä yhteydessä fytokannabinoidi kannabidioli,
joka tunnistettiin useita vuosikymmeniä sitten ja joka voi olla
vuorovaikutuksessa kannabinoidijärjestelmän kanssa, on lupaava molekyyli
farmakoterapiaa varten.
Suhteellisen
hiljattain on osoitettu monisuuntaisia biologisia vaikutuksia erilaisissa
prekliinisissä malleissa, mukaan lukien kannabidiolin antioksidanttiset ja
anti-inflammatoriset vaikutukset [14,73]. Edellä esitettyjen tietojen
perusteella CBD näyttää olevan suositeltavampi kuin muut fytokannabinoidien
ryhmään kuuluvat yhdisteet. Riippumatta itse CBD:n hyödyllisistä
farmakologisista vaikutuksista, jos tämä yhdiste on Δ9-THC-ympäristössä,
99-THC:n ei-toivotut vaikutukset vähenevät, mikä parantaa sen turvallisuusprofiilia
[132].
CBD:n
terapeuttisissa sovelluksissa on tärkeää, että sillä ei ole psykotrooppisia
vaikutuksia. Lisäksi tämä fytokannabinoidi ei ole teratogeeninen eikä
mutageeninen [133]. Viime aikoihin asti CBD:llä katsottiin olevan vain vähäinen
myrkyllisyys ihmisille ja muille lajeille [134], mutta viimeaikaiset
tutkimukset osoittavat ALT- ja AST-tasojen nousua CBD-hoidon jälkeen, mikä
sulkee sen pois valintalääkkeeksi [135,136]. Lisäksi on havaittu, että CBD voi
häiritä joidenkin lääkkeiden maksametaboliaa inaktivoimalla sytokromi P450
3A:ta ja P450 2C:tä [137]. Tällaiset yhteisvaikutukset on otettava huomioon,
kun CBD:tä annetaan samanaikaisesti muiden edellä mainittujen entsyymien
metaboloimien lääkkeiden kanssa.
Jotta
löydettäisiin yhdisteitä, joilla olisi CBD:tä parempi terapeuttinen profiili ja
aktiivisuus ilman haittavaikutuksia, tarkistettiin sekä luonnollisten että
synteettisten CBD-johdannaisten biologiset ominaisuudet ja toivottiin, että
löydettäisiin täydellinen johdannainen, joka tarjoaa lähes ihanteellisen
terapeuttisen vaikutuksen.
Kannaway info
https://kannaway.com/CorpOrphan/cbd,
CBD on yhä suositumpi. Vaikka se on yleistymässä terveys- ja hyvinvointimaailmassa, väärää tietoa on edelleen runsaasti. Keskeinen osa Kannawayn missiota on kouluttaa ihmisiä ympäri maailmaa, erityisesti kannabinoidien osalta.
Yksinkertaisesti selitettynä kannabidioli tai CBD, kuten se yleisemmin tunnetaan, on luonnollinen kasvitieteellinen tiiviste, joka kuuluu erilaisten yhdisteiden luokkaan, joita kutsutaan kannabinoideiksi. Nämä yhdisteet ovat peräisin sekä kannabiskasvien varsista että siemenistä. Kannawayn CBD on peräisin teollisuushamppua, ja lippulaivalähteemme on uskomaton viidennen sukupolven hampputilamme Euroopassa. Hamppukasvista on tähän mennessä tunnistettu yli 100 kannabinoidia, ja CBD on yksi tunnetuimmista.
CBD ei ole päihdyttävää, mikä tarkoittaa, että sillä on potentiaalia tuottaa erilaisia henkisiä ja fyysisiä hyötyjä ilman ei-toivottuja sivuvaikutuksia. Koska sana sen tehokkuudesta leviää kulovalkean tavoin, CBD:stä on tullut suosittu hyödyke luontaistuoteteollisuudessa. Tämä johtuu osittain siitä, että CBD, kuten muutkin kannabinoidit, on vuorovaikutuksessa kehon luonnollisesti esiintyvän endokannabinoidijärjestelmän kanssa, joka on vastuussa tasapainon edistämisestä ja sellaisten toimintojen säätelystä kuin ruokahalu, uni ja immuunivaste.